تروما چیست؟ و نحوه ارزیابی و احیا در مدیریت تروما چگونه است؟
نکات کلیدی:
- احیای اولیه بایستی بر ارزیابی و تثبیت سریع آسیب های تهدید کننده حیات با مدیریت آسیب های غیر تهدید کننده تا پایداری حالت بیمار متمرکز است.
- احیای کنترل آسیب شامل دسترسی وریدی موثر، اجتناب از هیپوترمی و احیای کلوییدی به جای کریستالوییدی می باشد.
- ارایه کننده ها بایستی قادر به درک علایم و نشانه های لوله گذاری اضطراری و اختیاری در شرایط تروما ونیز گزینه ها در زمانی که لوله گذاری امکان پذیر نیست
- ترکیب فیلم های ساده، معاینه فیزیکی و اولتراسوند امکان تریاژ کامل و شناسایی همه مکان های خونریزی همودینامیک را می دهد
- برگشت انسداد بالن آئورت در بیماران دارای فشار خون سودمند است با این حال مترادف با توراکوتومی احیاگر نیست.
کلمات کلیدی: ارزیابی تروما – احیا – بررسی اولیه – دسترسی وریدی، تریاژ حفره
مقدمه
ساعت طلایی اولین بار توسط آدامز کولی برای تاکید بر اهمیت مدیریت سریع و مدیریت کارامد بیماران اسیب دیده مطرح شد. پیشرفت ها در زمینه احیا و تشخیص طیف وسیعی از گزینه های رویه ای و تصویربرداری را در اختیار پزشکان ارایه کرده و منجر به مراقبت بهتر از تروما در همه سطوح شده است.
فراتر از پشتیبانی زندگی تروما:
احیای اولیه در اورژانس ها
مدیریت مجاری تنفسی، تنفس، گردش خون،معلولیت، مدیریت مواجهه که توسط ATLSآموزش داده می شود.یک چارچوب موثر برای ارزیابی و مدیریت اولیه بیمار بوده و موجب افزایش کارایی و کیفیت مراقبت می شود. در مرکز ترومای مجهز، این فرایند ها را می توان به طورموازی انجام داد. آن ها بیانگر ارزیابی کامل بیمار اسیب دیده به شکلی کارامد و منظم می باشد.
تروما چیست؟
آسیب تروماتیک اصطلاحی است که به آسیب های فیزیکی با شروع و شدت ناگهانی اشاره دارد که نیاز به مراقبت فوری پزشکی دارد. این آسیب یا ضربه ممکن است باعث شوک سیستمیک به نام “ترومای شوک” شود و ممکن است نیاز به احیا و مداخلات فوری برای نجات جان و اندام داشته باشد. صدمات تروماتیک نتیجه طیف گسترده ای از مکانیسم های بلانت، نافذ و سوختگی است. آنها شامل برخورد وسایل نقلیه موتوری، آسیب های ورزشی، سقوط، بلایای طبیعی و بسیاری از آسیب های فیزیکی دیگر هستند که می توانند در خانه، خیابان، یا هنگام کار رخ دهند و نیاز به مراقبت فوری دارند.
بسیاری از حوادث منجر به آسیب تروماتیک را می توان به طور مناسب در بخش های اورژانس بیمارستان درمان کرد. صدمات تروماتیک شدیدتر و چندگانه ممکن است توسط تیم های آمبولانس 115یا هلیکوپتر به عنوان هشدار تروما تریاژ شود. هشدار تروما سطح یک تعیین بر اساس ارزیابی فیزیکی سریع نیازهای پزشکی فوری قربانی است. بر اساس معیارهای هشدار تروما، اولین پاسخ دهندگان بیمار را به مناسب ترین بیمارستان تحویل می دهند.
دستورالعمل های تروما در ایالات متحده برای اولین بار در سال 1976 ایجاد شد، و یک شبکه پیچیده تروما کارآمد اکنون به همه ما در هر کجا که زندگی می کنیم، کار می کنیم یا سفر می کنیم، خدمت می کند. بیمارستانها بر اساس مراقبتهایی که میتوانند ارائه کنند و همچنین حجم خدمات شهری و روستایی، بهعنوان مراکز تروما سطح I، II، III یا IV مشخص و تعیین میشوند. سیستم تروما برای تطبیق تلفات انبوه و موقعیت های فاجعه طراحی شده است. مراکز سطح I بالاترین سطح مراقبت را با منابع و قابلیت های بهینه، کارکنان و تخصص ها به صورت شبانه روزی ارائه می کنند و به طور مداوم تحت نظارت قرار می گیرند تا اطمینان حاصل شود که استانداردهای ملی را برآورده می کنند یا از آنها فراتر می روند. مراکز تروما از نزدیک با سیستم های EMS مربوطه خود کار می کنند تا مراقبت از قبل از بیمارستان آغاز شود.
بیمارانی که به شدت آسیب دیده اند که هشدار تروما در نظر گرفته می شود به یک منطقه احیا تحویل داده می شوند که ممکن است بیشتر شبیه اتاق عمل باشد تا یک بخش اورژانس سنتی. در این محیط، یک تیم حرفه ای تروما با مهارت بالا آماده ارائه روش های نجات جانی فوری در سوله های تروما پیشرفته است. تحقیقات نشان می دهد که رسیدن به مکان مناسب در زمان مناسب، که معمولا به عنوان “ساعت طلایی” یا 60 دقیقه اول پس از وقوع یک ترومای بزرگ چند سیستمی شناخته می شود، بسیار مهم است. جراحان ترومای بزرگسالان و اطفال، کارکنان تروما و منابع 24 ساعته و 7 روز هفته آماده ارائه این سطح منحصر به فرد از پاسخ هستند تا بیمارانی که به شدت آسیب دیده اند بهترین شانس ممکن برای زنده ماندن و کمترین ناتوانی باقیمانده از صدمات خود را داشته باشند.
پس از مراقبت در منطقه احیای تروما در یک مرکز سطح یک، بیماران ممکن است به عمل جراحی، بخش مراقبت های ویژه یا طبقه پرستاری تروما، با تمام منابع و خدمات بیمارستان در یک روش چند رشته ای واقعی در دسترس باشند. بیمارانی که به مراکز سطح II-IV آورده می شوند ممکن است در آن بیمارستان بمانند یا در صورت لزوم به سطح بالاتر مراقبت منتقل شوند.
انواع آسیب های تروماتیک
برخی از انواع متداول آسیب های تروماتیک عبارتند از، اما محدود به موارد زیر نیست:
آسیب تروماتیک مغز
آسیب نخاعی
شکستگی ستون فقرات
قطع عضو – تروماتیک
ضربه به صورت
ترومای صوتی
آسیب له شدگی
ضربه مغزی
استخوان شکسته
فک – شکسته یا دررفته
شکستگی جمجمه
بریدگی و سوراخ شدگی زخم ها
کوفتگی میوکارد
آسیب الکتریکی
شوک هیپوولمیک
خونریزی زیر عنکبوتیه
هماتوم ساب دورال
⚕️معاینه سریع تروما
معاینه سریع تروما یعنی مشاهده سریع،لمس مناطق حیاتی بدن بیمار و شناسایی آسیب های تهدید کننده حیات که در بررسی اولیه مشخص می شود. طی بررسی ترومای سریع،شما بایدسر،گردن،قفسه سینه،شکم،لگن،اندام ها و پشت بیمار را ببینید و اختصار DCAP-BTLS را بخاطر بسپارید:
D:Deformity
حالت غیر طبیعی در شکل و اندازه بدن خصوصا استخوان ها ی شکسته،مفصل دررفته و تورم
C:Contusion or Crepitus
کنتوژن در اثرخونریزی زیر پوست ایجادشده و مشخه آن تغییر رنگ پوست است،کریپتوس یک صدای ساینده مانند آنچه در اثر استخوان های شکسته یا آمفیزم زیر پوستی شنیده می شود
A:Abration
خراش در اثر اصطکاک
P:Penetrating Trauma
ترومای نافذ که باعث سوراخ شدن پوست می شوند
B:Burn
سوختگی،تخریب بافتی است که در اثر تماس شیمیایی،الکتریکی یا حرارتی ایجاد می کند
T:Tendernes
دردی که در اثر لمس ایجاد می شود
L:Laceration
لاسراسیون بریدگی پوست است که می تواند دندانه دار یا خیلی صاف باشد و وابسته به جسمی است که آن را ایجادکرده است
S:Swelling
تورم،بزرگ شدن بخشی از بدن است که در اثر تجمع خون یا سایر مایعات بدن در بافت های آسیب ایجاد می شود
دسترسی/مجاری هوا
دسترسی وریدی
اگرچه معمولا ساده است، دسترسی وریدی یک مسئله سخت در مراقبت ازبیمار تروما است. احیای استاندارد مستلزم قرار دادن IV در موقعیت ضد انعقاد با کمک اولتراسوند می باشد. جایگزین های تزریق محیطی در صورتی باید انجام شود که به طور سریع تکمیل شود. چندین گزینه برای دسترسی مورد استفاده در تروما می باشند و تغییراتی در سرعت تجویز مایع وجود دارد. راه حل های دیگر نظیر کوتاه کردن وریدی ، کاتتریزاسیون 4، کاتتریزاسیون مستقیم مستقیم دهلیس و کتتریزاسیون ورید ناف در نوزادان، را می توان در نظر گرفت.
کاتتریزاسیون وریدی مرکزی
کاتتریزاسیون وریدی مرکزی (CVC) یک روش کارآمد برای دسترسی به عروق است. دسترسی به سابلووا یا فمورال اغلب به دلیل سهولت قرار دادن بدون دستور العمل ایالات متحده، ترجیح داده می شود. هنگام استفاده از دسترسی فمورال به محدوده ترومای شدید به قفسه سینه یا شکم، به خصوص آسیب های نفوذی، باید با احتیاط حفظ شود، زیرا اختلال یا آسیب ناشی از وریدی یا رگهای خلفی باعث جلوگیری از تحویل کافی می شود. علاوه بر این، در مورد دسترسی شریانی، این خطوط را می توان در موارد اضطراری استفاده کرد، اما باید سریعا به دسترسی ورید تبدیل شود.
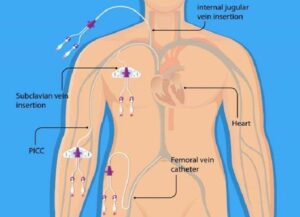
کاتتر داخل وریدی
کاتتر داخل وریدی در احیای تروما پذیرفته شده و جایگزین سریع برای CVS می باشد. در بیماران ترومای بالغ، دسترسی هومورال و تیبیال با نرخ موفقیت بیش از 97 درصد گزارش شده است واین در حالی است که مکان های دیگر نظیراسترنوم، قله ییلیاک و فمور توصیف شده است.
| باکس 1: ترومای استاندارد |
| 1. ورود بیمار
2. بررسی پالس الف دسترسی IV ب اندازه گیری دستی فشار خون 3. بررسی اولیه 4. گزارش خدمات اورژانس پزشکی 5. تصویربرداری افزاینده 6. بررسی دوم 7. وضعیت |
| باکس 2: نرخ اینفیوژن کاتتر ها |
| هومورال 80 میلی لیتر بر دقیقه
تیبیال 15 میلی لیتر بر دقیقه 32 میلی متر 14 گرم IV 325 میلی لیتر در دقیقه 30 میلی متر 16 گرم IV 215 میلی لیتر در دقیقه 30 میلیمتر 18 گرم IV 110 میلی لیتر در دقیقه 30 میلی متر 20 گرم IV 63 mL / min بندر 9 Fr Mac دشتال 508 میلی لیتر در دقیقه Proximal 200 mL / min 8.5-F Cordis 125 mL / min پروتز دیستال لومی سه فاز 7-F، 38 mL / min متوسط 17 میلی لیتر در دقیقه |
به علاوه، احیا از طریق IO هومورال به رگ زیر کلواوی می شود که درنهایت موجب تسهیل قرار گیری CVC می شود.
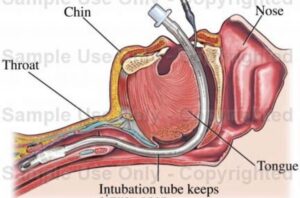
مجرای هوا
علایم لوله گذاری: در طی ارزیای اولیه بیمار اسیب دیده، بایستی در خصوص کنترل مجاری هوا تصمیم گیری شود. برای تسهیل این، اتحادیه جراحی تروما، دستورالعمل هایی را برای علایم لوله گذاری تروما ارایه کرده است
| جدول 3: علایم لوله گذاری اصطراری |
| لوله گذاری اضطراری
انسداد راه هوایی هیپوتنوسیون هیپوکسمی 90٪ اختلال شناختی شدید (GCS؟ 8) شوک و خونریزی شدید سکته قلبی سوزش عمده (40٪) یا آسیب استنشاقی لوله گذاری انعطاف پذیر ترومای صورت یا گردن اختلال شناختی متوسط (GCS 9-12) مبارزه پایدار مقاوم در برابر مداخلات دارویی ناراحتی تنفسی آسیب نخاعی گردنی |
اگرچه بیماران با مقیاس کما گلاسکو 8 یا کم تر نیازمند لوله گذاری است، مقیاس کما گلاسکو 9-12 مربوط به 33 درصد اسیب مغزی تروما بوده ویا این که با 12.7 درصد TBi همراه است. تلاش های منطقی بایستی برای پشتیبانی از تهویه غیر تهاجمی در بیماران tbi صورت گیرد . تلاش های منطقی بایستی برای کنترل اشفتگی در این شرایط برای اجتناب از مشکل همودینامیک و نیزخطر هیپوکسی مربوط به لوله گذاری صورت گیرد. اگر این روش ها ناموفق باشند،لوله گذاری برای تسریع ct و مدیریت TBI لازم است. به طور مشابه، بیماران با اسیب نخاع گردن ممکن است مشکلات تنفسی داشته باشند و از لوله گذاری بهره مند شوند و این می تواند در تروما در نظر گرفته شود.
عوامل القایی برای لوله گذاری اضطراری: لوله گذاری سریع بایستی برای همه شرایط اضطراری در تروما استفاده شود. هیچ گونه داده شفافی برای پشتیبانی از اولویت رژیم دارویی وجود ندارد. سوکسینیل کولین عامل تخفیفی ترجیح داده می شود، اگرچه سوکین سیلین کولین به علت سوختگی قابل توجهی، آسیب های آسیب دیده، مدت زمان طولانی یا نارسایی کلیوی مورد استفاده قرار می گیرد. یک پروتکل پیشنهاد شده در باکس 4 بررسی شده است. تمرینکنندگان باید با هر دو رژیم دوز IV و عضلانی آشنا باشند و یا باید آنها را به صورت واضح در خلال تروما نمایش داد. در این پروتکل، کتامین، داروهای القا شده ترجیحی برای مشخصات مطلوب همودینامیک و سهولت دوز است. اگرچه یک زمانی TBI ضد کتامین در نظر گرفته می شد، ولی این مسائل رد نشده اند. تمام داروهای القاء، از جمله کتامین، ممکن است به دلیل تخلیه پاسخ سمپاتیک به تروما باعث ایجاد همودینامیک شوند. ، در شرایط فشار خون شدید، بیماران ممکن است از تهویه غیر تهاجمی بهره مند شوند تا پروتکل های انتقال عظیم برای جلوگیری از فروپاشی همودینامیک کامل به کار گرفته شود.
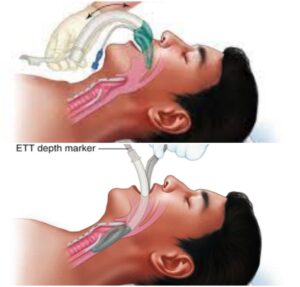
جایگزین هایی برای لارنگوسکوپی مستقیم برای لوله گذاری سخت: اگر چه لارنگوسکوپی مستقیم (DL) مکانیسم ترجیحی لوله گذاری است، جایگزین های متعددی توسعه یافته است و باید براساس آشنایی و تجربه آنها در نظر گرفته شود. همه پروتوکل های احیا شامل جایگزین های DL در تروما به دلیل عوامل متعددی است که موجب افزایش سختی انکوباسیون اضطراری می شود.
| باکس 4: گزینه های لوله گذاری ترتیبی سریع |
| عامل القاء ترجیحی
کتامین 1 تا 3 میلی گرم بر کیلوگرم IV پروپوفول 60 تا 200 میلی گرم (20-20 سانتیمتر) اتامید 10 تا 20 میلی گرم IV (10-5 سانتیمتر) وسوکسینیل کولین 80 تا 100 میلی گرم (4-5 سانتیمتر) اگر قادر به دسترسی به IV / IO نباشید: کتامین 5 میلی گرم بر کیلوگرم IM وسوکسینیل کولین 5 mg / kg IM |
لارینگوسکوپی ویدئویی
لارینگوسکوپی ویدئویی مزایای زیادی نسبت بهDL دارد و بایستی گزینه ای برای لوله گذاری باشد. مزیت اصلی سهولت نظارت بر افراد بی تجربه است اگرچه VL ازنظر مدیریت بیماران جاق و بیماران با اسیب نخاعی مشکوک کاربرد بیشتری دارد. VL ممکن است در مقایسه با DL در مقایسه با DL بهبود یافته باشد، به طوری که باعث کاهش احتمال بروز هیپوکسی در انتوباسیون اضطراری شود. این ممکن است به لحاظ نظری برای آسیب نخاعی یا بیمار TBI مفید باشد اما این به طور بالینی نشان داده نشده است. تمرینکنندگان باید حداقل با گزینه های VL در مراکز خود آشنا شوند.

دستگاه های سوپراگلوتیک
دستگاه های سوپراگلوتیک ، از جمله ماسک حنجره، Combitube (Medtronic، Minneapolis MN، ایالات متحده آمریکا) و کینگ امبو ، دانمارک) ایروی (همچنین به عنوان راه های هوایی مری یا مسیریابی نامیده می شود) معمولا به عنوان ابزار نجات توسط هر دو در بیمارستان و ارائه دهندگان بیمارستانی ارایه می شود. هیچ دستگاهی برتر از دستگاه دیگر نیست و انتخاب دستگاه بر اساس اشنایی است. این دستگاه ها دارای اهمیت کمی در تروما هستند زیرا بیماران اسیب دیده دارای ریسک بی خوابی هستند. علاوه بر این، زمانی که لوله گذاری داخل تراشه به علت راه هوایی یا ادم بند ناف آواری امکان پذیر نیست، دستگاه های سوپراگلوتیک نیز مناسب نیستند. دستگاه های سوپراگلوتیک نباید در معرض هواپیما با دوام باشند و باید همانند زود به لوله تراشه یا راه هوایی جراحی تبدیل شوند. بیمارانی که دستگاه های سوپراگلوتیک را در این زمینه دریافت می کنند، باید در خلای تروما مورد ارزیابی قرار گیرند و اگرچه گزینه ای مناسب در تنظیم پیش دندانپزشکی است ،ولی باید از آسیب های احتمالی آن جلوگیری شود
مجاری جراحی
همه بیمارانی که لوله گذاری اندوتراکئال در آن ها با شکست مواجه شده است بایستی برای جراحی اماده شوند. تراکئوستومی اورژانسی باید برای بیمارانی که بدون لوله گذاری به خوبی تهویه دارند، رزرو شود. هر دو کراتوتیروئیدوتومی و تراکئوستومی ممکن است انجام شود، و هر دو ممکن است بسته به تجربه جراح، باز و یا پوستی انجام شوند. اگر چه بعضی از داده ها نشان داده اند که کری کتی تروییدوتومی اورژانسی برای کنترل کوتاه مدت نیازی به تجدید نظر ندارد، باید مشخص شود که بیمار باید تشخیص دهد. به طور حاد، کراتوتیروئیدوتومی بیشتر احتمال دارد به طور تصادفی باشد بیمارانی که در معرض خطر ابتلا به چندین بیماری هستند، بیمارانی که نیاز به چندین روش دارند، یا کسانی که ممکن است تحریک شوند و دچار مشکل شوند. در این بیماران تراکئوستومی ممکن است گزینه ترجیحی و ایمن تر باشد، اگر همودینامیک آنها امکان تبدیل را فراهم کند.
تنفس و تهویه
داده های کمی وجود دارند که راهبرد های تهویه ای اولیه را برای بیماران تروما پشتیبانی کنند و این در حالی است که لوله گذاری در این گروه بر اساس پروتوکل های خاصی برای لوله گذاری انحصاری است. استفاده از دستگاه تهویه با راهبرد حفاظت از ریه میتواند مطلوب باشد. یک فرا تحلیل نشان داد که شروع تهویه با حجم ایده ال 6 تا8 کیلوگرم در برابر تهویه حجم بالا در بیماران اورژانسی موجبکاهش میزان اسیب ریوی ، عفونت کلیوی و مرگ و میر می شود. انتقال این داده ها به جمعیت تروما محدود است و باید توجه داشت که تهویه حفاظتی با افزایش PaCO2 همراه است و همچنین نیاز به فشار مثبت و منفی بالایی دارد که هر دو ممکن است به زیر گروه های مختلف آسیب رسانده باشند جمعیت 11 ساله و ممکن است نیاز به آرامسازی بیشتری برای تسهیل استراتژی محافظت کم حجم داشته باشد. 12 آزمایش در حال انجام استراتژی های تهویه می باشد. . پزشکان باید قضاوت بالینی را در تعیین یک استراتژی تهویه کننده برای بیمار مبتلا به تروما انجام دهند.
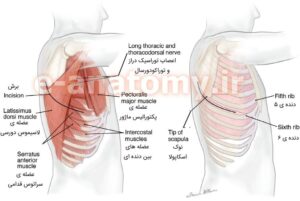
آسیب به سینه
اکرچه اسیب های زیاد به سینه در این مقاله بررسی شده است با این حال هموراکساکس با اسیب های اولیه در بیماران دارای فشار خون همراه بوده است. زهکشی لوله سینه باید در خلای تروما برای کمک به تریاژ اوراسیا ارائه شود. هموتاوراکس اغلب سایر آسیب های قابل توجهی در قفسه سینه را پیش بینی می کند و این بیماران باید برای صدمات عروق، ریه و قلب بزرگ مورد ارزیابی قرار گیرند. به علت فشار منفی در قفسه سینه، افیوژن پریکارد یک شاخص حساس به اندازه کافی از آسیب های قلبی در بیماران مبتلا به هموتوراکس است و آسیب های قابل توجه در قلب ممکن است در ، CT یا اکوکاردیوگرافی باشد
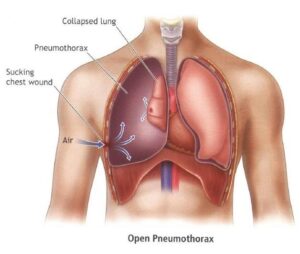
پنوموتوراکس
پنوموتوراکس قادر به مدیریت اورژانسی نبیست ولی در حضور فیزیولوژی فشار خون، مداخله در طی جراحی اولیه اجباری است. سه روش فشرده سازی اضطراری در اختیار سازنده قرار می گیرد. فشردن سوزن یک گزینه قابل قبول است، اگر چه گزینه های دیگر نیز وجود دارد . فشرده سازی سوزن می تواند در بسیاری از بیماران به دلیل موقعیت نامناسب، انسداد یا جابجایی نامناسب باشد. مدل های کاداور نشان داده اند که یک موقعیت مادون قرمز ممکن است به دلیل تفاوت در ضخامت قفسه سینه در یک جمعیت آمریکایی باشد. گزینه با دوام بیشتر شامل توراکوستومی انگشتی و قرار دادن لوله رسمی سینه. توراکوستومی انگشتی بعدا تبدیل به لوله سینه است ، اما در شرایط حساس زمانی موثر است. انتخاب اندازه لوله سینه به طور قابل توجهی ثابت نشده است، قرار دادن توراکوتومی لوله از طریق پوست ممکن است گزینه درمانی مناسب باشد، اما برای بیمار ناپایدار به دلیل نگرانی در مورد انسداد لوله و آگاهی از عملکرد لوله ها مطلوب است.
اجتناب از هیپوترمی
هیپوترمی دارای اثر منفی بر روی برایند ها در اسیب تروما است و بیماران دارای برایند های بهتری از احیا می باشند. تغییرات معنی دار انعقاد در دمای 35 درجه شروع می شود. مکانیسم های مختلف شناسایی شده اند که شامل مهار مستقیم از آبشار انعقاد، تغییرات مورفولوژیکی به پلاکتها، کاهش تجمع پلاکتها و ترومبوز مایع منجمد است. در بیماران باهیپوترمیمتوسط، اثرات پلاتت یکی از علل رایج کوگلوپاتی بوده است و اثرات موجب تاخیر در انعقاد می شود. افت حرارتی در بیماران تروما از 60 کیلوکالری تا 400 کیلوکالری پس از ترومای حد افزایش می یابد. به این ترتیب تلاش هایی در طول دوره احیا برای اجتناب از هیپرترمی لازم است. ارزیابی اخیر بانک داده های تروما عوارض عفونی وترومبوز را برای بیماران با هیپرترمی نشان داده است. با افزایش شدت هیپرترمی، مداخلات تهاجمیبایستی شروع شود که شامل استفاده از پد حرارتی و نیز هوای مرطوب و گرم است. هیپرترمی عمیق نیازمند گزینه های بنیادین از جمله لارو حفره حفره گرما، گرم شدن عصبی مصنوعی از طریق اکسیژن غشای خارج شده یا مدارهای همودیالیز، 21 یا سیست کاتتر تجدید عروق فعال است.
فشار خون
اگرچه مداخلات پیش بیمارستانی در این مقاله بحث شده است، استفاده از احیای کنترل اسیب یا فشار خون پایین، برتر ازراهبرد های احیای مجدد بوده است. فشار خون سیتوسولیک هدف 90 میلی مترجیوه برای پرفیوژن کافی در بیماران اسیب دیده کافی است و احیای مجدد کریستالویید بایستی محدود باشد. احیاء سیگنال در 250 تا 500 میلی لیتر عصاره جیوه می تواند برای حفظ فشار خون مناسب سیستولیک یا وجود پالس شعاعی استفاده شود. از لحاظ تئوری کاهش استفاده از کریستالوئید مانع از افزایش انعقاد در رقیق شدن عوامل لخته شده، تشدید هیپوترمی و اسیدوز ، و افزایش خونریزی از فشار هیدرواستاتیک میشود . موارد منع از هیپوتانسیون مجاز عبارتند از: سالمندی، آسیب های سر، حاملگی، و تخلیه طولانی مدت و یا زمان به علت آسیب های ناشی از هیپوتانسیون مداوم در این گروه ها. این استراتژی باید تا زمانیکه کنترل قطعی خونریزی صورت گیرد استفاده شود.علاوه بر استفاده از فشار خون در TBI، که در آت فشار خون مرتبط با برایند های عصبی است، در این سناریو، مدیریت بایستی بر حفاظت از بافت مغزی متمرکز شود و فشار خون باید در برابر اسیب عصبی کاهش یابد.در فشار خون سیتوسولیک بالا، نیرو های هیدرواستاتیک موجب تشدیدادمای مغزی بوده و با عواملی کنترل می شود که موجب افزایش اتساع مغزی نمی شود.
توراکوتومی احیا ی مجدد
علی رغم ارزیابی دقیق توراکوتومی احیا ی مجدد به عنوان یک مانور نجات، بحث های زیادی در خصوص استفاده از آن وجود دارد. دستور العمل های فعلی بر مکانیسم و زمان متمرکز است زیرا در نفوذ اسیب با مدت زمان انتقال کوتاه سودمنداست. این مداخله پس از ترومای بلانت سودمند است زیرا بقا در این گروه کم بوده و خطر استفاده و بهرهبرداری از منابع بالا است.هیچ گونه توصیه ای در خصوص سن بیمار وجود ندارد اگرچه توراکتومی دارای نرخ بقای مشابهی است. به علاوه، تشخیص های جدید نظیر US و CO2 تیدال، در تعیین این مسئله مفید است. استفاده از این روش ها در دستور العمل های خاص ارایه شده است اگرچه بسیاری از جراحان تروما از ان ها برای تعیین RT استفاده کرده اند.
انسداد بالن احیا گر ائورت
این فرایند جایگزین RT در انتخاب بیماران می باشد که معمولا از زمان مشابه با دوره های دیگر استفادهمی کند اگرچه مخالفان بر این باورند که کمبود تجربه سازمانی و دستور العمل های مشخص مانع از کاربرد آن می شود.REBOA یک شیوه موثر برای کنترل خونریزی در سینه نیست ولی استفاده از آن برای بیمار با اسیب های لگنی و شکمی یک جایگزین موثر برای RT است. کاهش اندازه کاتتر وافزایش تجربه نقش مهمی در پیش گیری از تروما دارد. از نظر مفهومی REOBA مشابه با کلامپ ائورت است. دسترسی سرخرگی در سرخرگ فمورال ایجاد می شود و این با کمک US صورت می گیرد. در شرایط ترومای حاد، متخصصان اشنا بایستی استفاده شوند زیرا ممکن است تصویر برداری موجود نباشد. REBOA بر اساس منطقه تعریف می شود و از این روی از شریان زیر کلواوی سمت چپ به شریان سلیاک، منطقه 2 که از سلیاک به شریان های کلیوی گسترش می یابد، و منطقه 3 که از شریان های کلیوی به بیوفکریت آئورت گسترش می یابد.
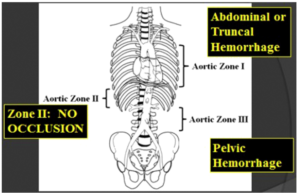
شکل 1: مناطق ائورتی برای »REBOA برای خونریزی شکمی یا تنه، بالون در ناحیه آئورت I نفوذ می کند؛ برای خونریزی لگن، بالون در منطقه III باد می شود. بالون نباید در منطقه II استفاده شود.
تصویر برداری سینه
رادیوگرافی قفسه سینه (CXR) باید به عنوان تریاژ اولیه قفسه سینه به دست آید، اما در نشان دادن هماتوثره های کوچکی ناکارآمد است و اغلب حتی ممکن است پنوموتوراکس قدامی را از دست دهد . اگر چه فیلمهای مستطیلی ممکن است زاویه کادوفنیک با ضخامت 400 سانتیمتر هموتوراکس داشته باشد ، فیلمهای ساق پا به طور قابل ملاحظه ای محدودتر است و ممکن است عملکرد ضعیف داشته باشد. اغلب، با این حال، CXR ممکن است تنها حالت موثر تصویربرداری موجود در زاویه حاده باشد و حتی با این محدودیت ها می تواند به طور موثر بلافاصله آسیب های زندگی خطرناک را شناسایی کند
اولتراسونوگرافی
اگرچه اولتراسونوگرافی توانایی محدودی در شناسایی اسیب های استخوانی به سینه وجود دارد ولی یک تست تشخیصی مطمئن برای پنوموتوراکس و هموتوراکس با حسایبت 60 تا 90 درصد باشد. در مقایسه با سی تی اسکن، اولتراسونوگرافی سریع تر است ولی از نظر تشخیص پنوموتوراکس ضعیف تر است. حساسیت اولتراسونوگرافی برای پنوموتوراکس بالا است و تشخیص این اختلال سریع تر از رادیوگرافهای ساده و یا سی تی اسکن می باشد.
توموگرافی کامپیوتری
سی تی اسکن حساسیت زیادی به دلیل اسیب حاد به سینه دارد اگر چه برخی از محققان استدلال کرده اند که این حساسیت ممکن است بیش از حد بالا باشد، بسیاری از شرایط غیر قابل انعطاف پذیری ریوی و پنوموتوراس های مخفی شناخته شده است. به همین ترتیب، همچنان استاندارد طلایی در بیمار پایدار در نظر گرفته می شود. با توجه به محدودیت زمانی و نیاز به حمل و نقل به بخش رادیولوژی، تصویربرداری سی تی به طور کلی فقط باید حساس به مایع باشد.
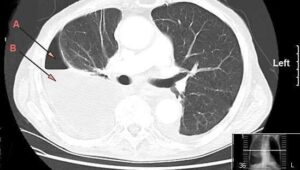
شیوه های تشخیص شکمی
سونوگرافی شکمی متمرکز برای تروما
FAST به یک استانداردی برای درمان و تشخیص سریع خونریزی درون شکمی تبدیل شده است و بایستی برای همه بیماران ناپایدار در معرض خطر اسیب شکمی استفاده شود. 200 سی سی هموپروتینئوم را می توان تا کم تر از 3 دقیقه بدون تروما شناسای کرد.حساسیت به این ماده 73 تا 88 درصد است. به عنوان یک شیوه تشخیصی برای تریاژ، اسیب کم تر از 200 سی سی خونریزی یکی از دلایل ناپایداری همودینامیک است.FAST قادر به اسیب به اندام های محکم نیست ولی برای بیماران با ترومای ثابت نیست سودمند نمی باشد.
توموگرافی رایانه ای
همانند ترومای سینه، سی تی اسکن یک شیوه تصویر برداری استاندارد طلایی برای بیمار تروما بوده و در نفوذ تروما و اسیب ها استفاده می شود. حساسیت برای اسیب درون شکمی بین 92 و 97.6 درصد اس و داده های ازمایشی نشان دهنده یک مقدار پیش بینی منفی بیش از 99.6 درصد است.
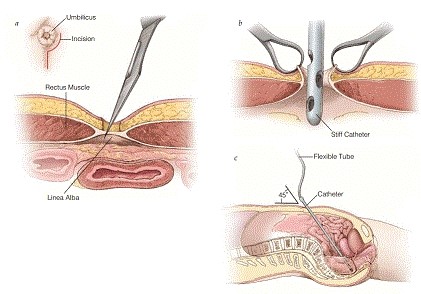
لاواژ تشخیصی پریتوان
استفاده از لاواژ تشخیصی پریتوان به شدت پس از ظهور FAST و افزایش دسترسی به سی تی اسکن کاهش یافته است. ارزش پیش بینی منفی DPL به طور معنی داری بیش از FAST است و صحت آن بالای 92 تا 98 درصد است و حساس تر از CT است. با این حال DPL با نرخ بالای نتایج مثبت کاذب محدود است.
شکستگی لگن و فمور
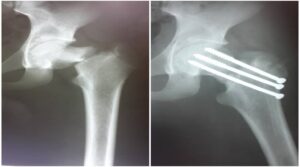
شکستگی لگن که بیانگر اسیب معنی دار همودینامیک می باشد در رادیوکراف ساده قابل شناسایی است. مطالعات کاداوار نشان داده است که دیاستاز بلوکی 5 سانتی متر موجب افزایش 20٪ در حجم لگن می شود در حالی که دیاستاز 10 سانتیمتری منجر به افزایش 40 درصدی می شود که نشان دهنده یک فضای بالقوه بالقوه برای از دست رفتن خون با آسیب به ورید های لگن است. استفاده از گیرنده های لگنی برای کاهش حجم لگن و کاهش نیازهای انتقال خون استFAST قادر به شناسایی اسیب است ولی نمی تواند برای حذف این اسیب ها کافی باشد. در بیمار ناپایدار همودینامیکبا شکستکی لگن،DPL موجب حذف خونریزی با شکستگی لگن می شود. در این شرایط می توان از سی تی اسکن استفاده کرد. بیماران با اختلال کنتراست بدون توجه به الگوی شکستگی لگن، در سی تی اسکن باید آنژیوآمبولیزاسیون انجام شود. علاوه بر این، هماتوم های لگنی که بیشتر از 500 سی سی هستند، خطر تقریبا 5 برابر نسبت به آسیب شریانی همراه دارند و باید با آنژیوگرافی تاخیر به آنژیوگرافی در بیماران همودینامیک ناپایدار با شکستگی های لگن صورت گیرد. شکستگی فمور یکی از منابع کاهش خون یا از دست رفتن خون با مطالعه شکستگی فمور با بیش از 12000 سی سی باشد. معاینه فیزیکی همراه با رادیوگراف ران برای حذف اسیب فمور برای تریاژ کافی است. برای بیمارانی که فاقد اسیب های تهدید کننده عمر است،
توصیه می شود که آن ها در24 ساعت تحت تثبیت قرارکیرند تا از دست رفت خون کاهش یابد.
خلاصه
ارزیابی اولیه بیمار تروما مستلزم هماهنگسازی تیم چند رشته ای باهدف شناسایی اسیب های تهدید کننده حیات و مداخله در خصوص برنامه های درمانی برای بیماران است.این یک دوره درمانی شدید بوده و تریاژ مستلزم منابعی برای کاهش مرگ ومیر است. به منظور ارایه بهترین مراقبت های درمانی ،پزشک باید بداند که چه منابعی موجود است و بتواند مراقبت های درمانی را به شیوه ای موثر در نظر بگیرد. این هماهنگی مراقبتی و درمانی نیازمند اموزش و تمرین با هدف نهایی نجات زندگی در طی ساعت طلایی احیا است.
REFERENCES
American College of Surgeons. Advanced trauma life support: ATLS; student
Course manual. 9th edition. Chicago: American College of Surgeons; 2012.
Tsang B, McKee J, Engels PT, et al. Compliance to advanced trauma life support
Protocols in adult trauma patients in the acute setting. World J Emerg Surg 2013:8(1):39
Assessment and Resuscitation in Trauma Management 995
Young J, Gondek S, Kahn S, et al. Challenging IV access in the patient with septic
shock. In: Diaz JJ, Efron DT, editors. Complications in acute care surgery: the
management of difficult clinical scenarios. 2017. Available at: http://lib.myilibrary.com?id5971614. Accessed March 14, 2017.
Bradley M. Brief report: systemic vascular access and resuscitation via corpus
cavernosum. Mil Med 2016;181(11):e1491–4.
Mayglothling J, Duane TM, Gibbs M, et al. Emergency tracheal intubation imme-
diately following traumatic injury: an Eastern Association for the Surgery of Trauma practice management guideline. J Trauma Acute Care Surg 2012;73(5 Suppl 4):S333–40.
Sise MJ, Shackford SR, Sise CB, et al. Early intubation in the management of trauma patients: indications and outcomes in 1,000 consecutive patients.J Trauma 2009;66(1):32–9, 40.
Como JJ, Sutton ERH, McCunn M, et al. Characterizing the need for mechanical ventilation following cervical spinal cord injury with neurologic deficit. J Trauma 2005;59(4):912–6 [discussion: 916].
Hassid VJ, Schinco MA, Tepas JJ, et al. Definitive establishment of airway control is critical for optimal outcome in lower cervical spinal cord injury. J Trauma 2008;65(6):1328–32.
Velmahos GC, Toutouzas K, Chan L, et al. Intubation after cervical spinal cord
injury: to be done selectively or routinely? Am Surg 2003;69(10):891–4.
Zeiler FA, Teitelbaum J, West M, et al. The ketamine effect on ICP in traumatic brain injury. Neurocrit Care 2014;21(1):163–73.
Neto AS, Simonis FD, Barbas CSV, et al. Lung-protective ventilation with low tidal volumes and the occurrence of pulmonary complications in patients without acute respiratory distress syndrome: a systematic review and individual patient data analysis. Crit Care Med 2015;43(10):2155–63.
Ferguson ND. Low tidal volumes for all? JAMA 2012;308(16):1689–90.
Fuller BM, Ferguson IT, Mohr NM, et al. Lung-protective ventilation initiated in the emergency department (LOV-ED): a quasi-experimental, before-after trial. Ann Emerg Med 2017. [Epub ahead of print].
Schroeder E, Valdez C, Krauthamer A, et al. Average chest wall thickness at two anatomic locations in trauma patients. Injury 2013;44(9):1183–5.
Inaba K, Lustenberger T, Recinos G, et al. Does size matter? A prospective anal-ysis of 28-32 versus 36-40 French chest tube size in trauma. J Trauma Acute CareSurg 2012;72(2):422–7.
Gentilello LM, Jurkovich GJ, Stark MS, et al. Is hypothermia in the victim of major trauma protective or harmful? A randomized, prospective study. Ann Surg 1997;226(4):439–47, 449.
Sharrock AE, Midwinter M. Damage control – trauma care in the first hour and beyond: a clinical review of relevant developments in the ield of trauma care.Ann R Coll Surg Engl 2013;95(3):177–83.
Lier H, Krep H, Schroeder S, et al. Preconditions of hemostasis in trauma: a re-view. The influence of acidosis, hypocalcemia, anemia, and hypothermia on func-tional hemostasis in trauma. J Trauma 2008;65(4):951–60.
Peng RY, Bongard FS. Hypothermia in trauma patients. J Am Coll Surg 1999;188(6):685–96.
Shafi S, Elliott AC, Gentilello L. Is hypothermia simply a marker of shock and injury severity or an independent risk factor for mortality in trauma patients? Analysis of a large national trauma registry. J Trauma 2005;59(5):1081–5.
Perlman R, Callum J, Laflamme C, et al. A recommended early goal-directed Management guideline for the prevention of hypothermia-related transfusion,Morbidity, and mortality in severely injured trauma patients. Crit Care 2016;20(1):107.
Kiridume K, Hifumi T, Kawakita K, et al. Clinical experience with an active intra-Vascular rewarming technique for near-severe hypothermia associated with trau-Matic injury. J Intensive Care 2014;2(1):11.
Bickell WH, Wall MJ, Pepe PE, et al. Immediate versus delayed fluid resuscitation For hypotensive patients with penetrating torso injuries. N Engl J Med 1994;331(17):1105–9.
Dutton RP, Mackenzie CF, Scalea TM. Hypotensive resuscitation during active-Hemorrhage: impact on in-hospital mortality. J Trauma 2002;52(6):1141–6.
Duchesne JC, McSwain NE, Cotton BA, et al. Damage control resuscitation: the New face of damage control. J Trauma 2010;69(4):976–90.
Stahel PF, Smith WR, Moore EE. Current trends in resuscitation strategy for the Multiply injured patient. Injury 2009;40(Suppl 4):S27–35.
Chesnut RM, Marshall LF, Klauber MR, et al. The role of secondary brain injury in Determining outcome from severe head injury. J Trauma 1993;34(2):216–22.
Helmy A, Vizcaychipi M, Gupta AK. Traumatic brain injury: intensive care man Agement. Br J Anaesth 2007;99(1):32–42.
Burlew CC, Moore EE, Moore FA, et al. Western Trauma Association critical deci-Sions in trauma: resuscitative thoracotomy. J Trauma Acute Care Surg 2012;73(6):1359–63.
Seamon MJ, Haut ER, Van Arendonk K, et al. An evidence-based approach to Patient selection for emergency department thoracotomy: a practice manage-Ment guideline from the Eastern Association for the Surgery of Trauma.J Trauma Acute Care Surg 2015;79(1):159–73.
Ferrada P, Wolfe L, Anand RJ, et al. Use of limited transthoracic echocardiogra-Phy in patients with traumatic cardiac arrest decreases the rate of nontherapeutic Thoracotomy and hospital costs. J Ultrasound Med 2014;33(10):1829–32.
Dennis BM, Medvecz AJ, Gunter OL, et al. Survey of trauma surgeon practice of Emergency department thoracotomy. Am J Surg 2016;212(3):440–5.
Brenner ML, Moore LJ, DuBose JJ, et al. A clinical series of resuscitative endo-Vascular balloon occlusion of the aorta for hemorrhage control and resuscitation.J Trauma Acute Care Surg 2013;75(3):506–11.
Biffl WL, Fox CJ, Moore EE. The role of REBOA in the control of exsanguinating Torso hemorrhage. J Trauma Acute Care Surg 2015;78(5):1054–8.
DuBose JJ, Scalea TM, Brenner M, et al. The AAST prospective aortic occlusion For resuscitation in trauma and acute care surgery (AORTA) registry: data on Contemporary utilization and outcomes of aortic occlusion and resuscitative
Balloon occlusion of the aorta (REBOA). J Trauma Acute Care Surg 2016;81(3):409–19.
Napolitano LM. Resuscitative endovascular balloon occlusion of the aorta: indica-Tions, outcomes, and training. Crit Care Clin 2017;33(1):55–70.
Livingston DH, Lavery RF, Passannante MR, et al. Admission or observation is not Necessary after a negative abdominal computed tomographic scan in patients-With suspected blunt abdominal trauma: results of a prospective, multi-Institutional trial. J Trauma 1998;44(2):273–80, 282.
Velmahos GC, Demetriades D. Early thoracoscopy for the evacuation of un-Drained haemothorax. Eur J Surg 1999;165(10):924–9.Assessment and Resuscitation in Trauma Management 997
Mowery NT, Gunter OL, Collier BR, et al. Practice management guidelines for Management of hemothorax and occult pneumothorax. J Trauma 2011;70(2):510–8.
Soldati G, Testa A, Pignataro G, et al. The ultrasonographic deep sulcus sign in Traumatic pneumothorax. Ultrasound Med Biol 2006;32(8):1157–63.
Kwon A, Sorrells DL, Kurkchubasche AG, et al. Isolated computed tomography Diagnosis of pulmonary contusion does not correlate with increased morbidity.J Pediatr Surg 2006;41(1):78–82, 82.
Como JJ, Bokhari F, Chiu WC, et al. Practice management guidelines for selective Nonoperative management of penetrating abdominal trauma. J Trauma 2010;68(3):721–33.
Ceraldi CM, Waxman K. Computerized tomography as an indicator of isolated Mesenteric injury. A comparison with peritoneal lavage. Am Surg 1990;56(12):806–10.Baque´ P, Trojani C, Delotte J, et al. Anatomical consequences of “open-book”Pelvic ring disruption: a cadaver experimental study. Surg Radiol Anat 2005:27(6):487–90.Krieg JC, Mohr M, Ellis TJ, et al. Emergent stabilization of pelvic ring injuries by Controlled circumferential compression: a clinical trial. J Trauma 2005;59(3):659–64.
Stephen DJ, Kreder HJ, Day AC, et al. Early detection of arterial bleeding in acute.Pelvic trauma. J Trauma 1999;47(4):638–42.
Evers BM, Cryer HM, Miller FB. Pelvic fracture hemorrhage. Priorities in manage-Ment. Arch Surg 1989;124(4):422–4.
Cothren CC, Osborn PM, Moore EE, et al. Preperitonal pelvic packing for hemo-Dynamically unstable pelvic fractures: a paradigm shift. J Trauma 2007;62(4):834–9, 842.
Lieurance R, Benjamin JB, Rappaport WD. Blood loss and transfusion in patients With isolated femur fractures. J Orthop Trauma 1992;6(2):175–9.
Gandhi RR, Overton TL, Haut ER, et al. Optimal timing of femur fracture stabiliza-Tion in polytrauma patients: a practice management guideline from the Eastern
Association for the Surgery of Trauma. J Trauma Acute Care Surg 2014;77(5):787–95.998 Gondek et al
Downloaded for Anonymous User (n/a) at MOH Consortium -Shahrekord University from ClinicalKey.com by Elsevier on October 04,


